初三学霸经历成绩暴跌与躯体化症状发作后,营养微生态干预2个月助她恢复正常
作者:王曼
伴有躯体化症状的重度焦虑抑郁障碍
在12–18岁的青少年群体中,情绪障碍的临床表现往往呈现“去情绪化”特征,躯体化症状成为更常见、更突出的主诉。一项发表于《Journal of the American Academy of Child & Adolescent Psychiatry》的系统性综述纳入119项研究,发现超过60%的青少年抑郁症患者以反复头痛、腹痛、恶心、疲劳、睡眠障碍为主要就诊原因,而情绪症状常被家长或医生忽视。在认知尚未成熟、情绪调节能力有限的背景下,青少年更倾向于将内在的心理冲突(如学业压力、家庭矛盾、自我认同危机)转化为可被社会接受的“身体不适”,从而避免被贴上“情绪不稳定”或“心理有问题”的标签。当孩子反复诉说“肚子痛”“头好晕”“没力气”时,家长和医生更容易接受“这是身体出了问题”,而非“心理出了问题”。
研究表明,压力水平与躯体化程度之间存在显著关联,个体承受的压力越重,其身体不适的症状往往也越突出、越复杂。对于身处中高考等关键阶段的初高中生而言,在以成绩为主导的评价体系下,这种将心理痛苦“翻译”成身体信号的情况尤为常见。[1]
案例展示
在上海德济医院/青岛大学上海脑科医学中心神经科学“脑-肠轴”微生态诊疗中心,我们接触到越来越多因情绪与学习问题困扰的青少年。他们中不少孩子曾是令人羡慕的“学霸”,却在压力下状态骤降,甚至无法继续学业。14岁的初三女生媛媛(化名,是我朋友家的孩子)就是其中之一——她从成绩优异到因重度焦虑被迫休学,又在营养微生态干预后,短短两个月内重返课堂、恢复稳定。她的转变,不仅再次印证了“肠脑轴”在情绪与认知调节中的关键作用,更想给所有家长一个重要的提醒:孩子的情绪崩溃和学习倒退,根源可能远不止是“心理压力”或“意志不坚”,其背后往往存在着可探查、可干预的肠道菌群的失衡。
成绩下滑背后的“失控”:那些被忽略的躯体信号
媛媛一直是成绩拔尖的女孩,2025年9月,是她初三开学第一次考试,成绩仍然保持优秀。但此时,她已经开始间断出现手抖,尚能自行控制。10月15日,媛媛第二次考试后成绩突然下滑。考试成绩不理想加上老师的批评,成为了压垮她情绪的最后一根稻草。她在和老师沟通的过程中突然浑身发抖、呼吸急促、蹲下后倒地、口唇青紫,整个过程持续约30分钟,期间她手脚麻木,叫她听不见。此后,类似发作如影随形:班主任谈话时、居家时、甚至在她曾经擅长的体育课上,跑步和做仰卧起坐时都曾诱发,每次发作120急救,缓过来以后还会跟老师说给您添麻烦了。妈妈说:“媛媛懂事的让人心疼,总是一副乖乖的样子”。
与此同时,她的睡眠变得很差,入睡困难且多梦。考试对她来说已成噩梦,会出现撕书、看到试卷就头痛、手抖甚至躲到课桌下的情况。

主动求医,却被卡在了药物的副作用
在巨大痛苦下,是孩子意识到自己可能病了(她的好朋友也是类似的症状,目前已经休学在家),媛媛主动要求去看精神心理科。2025年11月4日,她在当地医院完成了心理评估,焦虑自评量表(SAS)和抑郁自评量表(SDS)均提示为重度,自杀风险评估(NGASR)为高风险。临床诊断为:重度焦虑、重度抑郁、躯体化障碍,高自杀风险。医生给予了盐酸舍曲林治疗,但用药后媛媛出现了上课时不自主发笑、胃肠道反应等副作用。患病以来,她食欲下降,身高165cm的她,体重已降至47公斤(标准体重58.88kg),呈现出明显的消耗状态。热爱学习的她虽然已经无法集中精力上学,但是依然对于学习没有放弃。

寻找根源:不仅是心理,更是身体的失衡
来找我那天,正是 11 月 8 日下午她上体育课做仰卧起坐时再次出现躯体化症状持续30min左右,孩子的爸爸紧急联系我,希望可以得到更好的治疗。
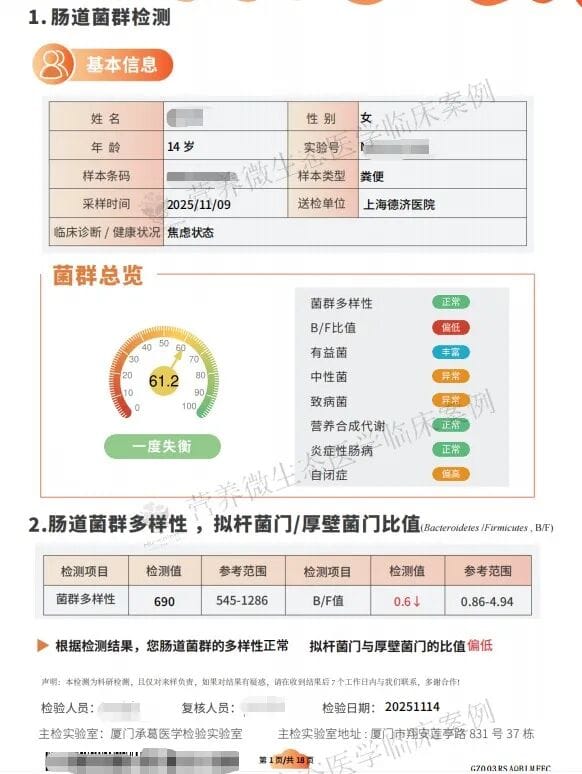
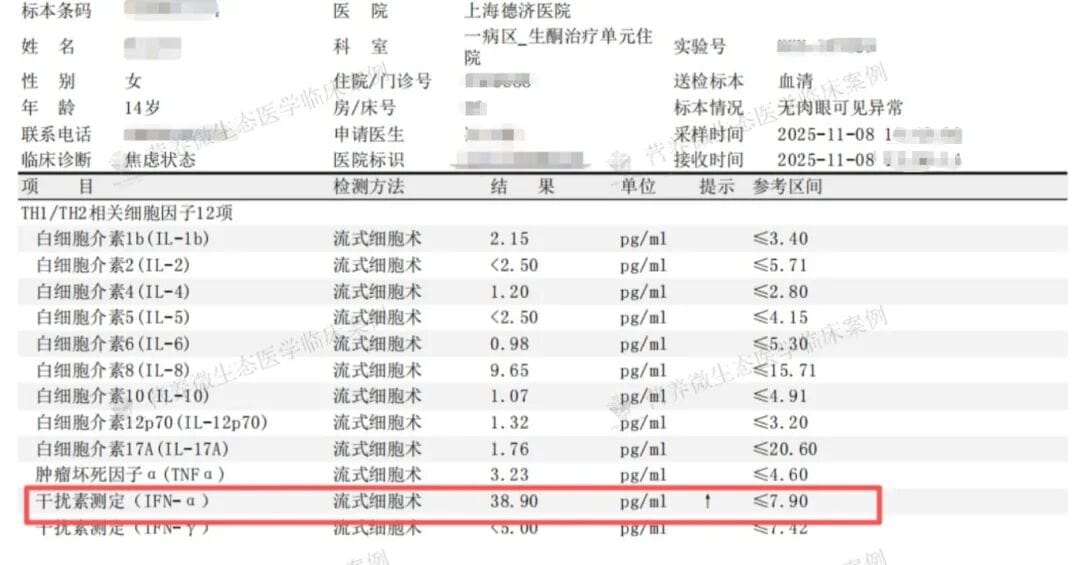
我首先为她安排了全睡眠周期高密度脑电生理定位监测,排除癫痫等神经系统器质性疾病的可能性 —— 这很关键,因为她的躯体发作容易被误诊。经了解,媛媛是足月顺产的第一胎,自幼发育正常,成绩优异,病后学习明显倒退。她的家庭变故(父母离异)或许也是她压力的来源之一。随后,我们将目光投向了近年来备受关注的“脑-肠轴”。肠道菌群检测结果提示她存在中度失调,其中核心有益菌拟杆菌的水平较低,出现了类似自闭的情绪障碍。同时,她的维生素D水平仅为29.95 nmol/L,属于明显缺乏状态。干扰素α(IFN-α)显著升高(38.9,参考值<7.9),升高近5倍,这并非单纯心理因素所致,而是强烈提示心身-免疫交互障碍的存在,异常升高的干扰素α,它不再仅作为外周免疫信号,而是通过多种途径穿透血脑屏障(BBB),进入中枢神经系统(CNS),引发神经炎症反应。这几个关键的指标异常,为我们理解她的病情提供了新的视角:持续的压力可能摧毁了她的肠道微生态平衡与营养状态,而这种失衡又反过来加剧了情绪的崩溃和躯体的症状。
2个月的调理:是她恢复正常学习的 “组合拳”
针对媛媛的情况,我和她的父母进行了详谈,精神类的药物家长拒绝使用,希望能有更好的方法,最好能短期内起效,并且有治愈的方法。我给她制定了营养微生态综合调理方案:首先是益生菌,选用含脆弱拟杆菌 BF839、朱红硫磺菌 ttys-997 等 11 种菌株的制剂,11 月 9 日开始每天 1 袋,但两天后她又发作一次,于是调整为每天 3 袋;其次,补充维生素 D3-K2(每天 1 万单位),同时搭配 “学霸镁”—— 苏糖酸镁、牛磺酸镁、甘氨酸镁复合制剂,每天 200mg(因为 D3 需要镁才能有效吸收和发挥作用);最后,加上复合 B 族维生素,支持神经功能修复。
自2025年11月中旬进行方案强化调整后,媛媛的发作性症状得到了彻底控制。2026年1月9日随访时,家长反馈她未再出现任何之前的发作症状,已经能够正常上学,情绪保持稳定。家长说真的不能想象孩子的精神如果不能恢复正常,以后会怎样,原计划的市重点高中的中考计划都不能奢望了,她班级有另外一个这样的孩子,是媛媛的好朋友,目前已经休学在家。
专业分析
重度情绪障碍与躯体化症状,绝非单纯的心理问题,而是社会心理压力通过“脑-肠轴”等生理通路,引发全身系统性紊乱的终末表现。
干扰素α升高与情绪障碍的潜在关联[2]:主要体现在以下三个方面:
1.神经递质紊乱:干扰素α可导致大脑中5-羟色胺(血清素)、多巴胺和去甲肾上腺素等关键情绪调节神经递质的合成减少或分解增加,尤其是5-羟色胺系统的耗竭,与抑郁、焦虑的发生密切相关。
2.神经内分泌改变:干扰素α能激活下丘脑-垂体-肾上腺轴(HPA轴),引起皮质醇水平升高,长期应激状态会加剧情绪不稳、疲劳和睡眠障碍。
3.神经炎症反应:高水平的干扰素α可能诱发轻度慢性神经炎症,影响前额叶皮层和边缘系统功能,导致认知迟缓、情绪低落和易激惹。
长期心理应激持续激活下丘脑-垂体-肾上腺轴(HPA轴),导致皮质醇节律紊乱[3]。这种慢性的应激状态直接破坏肠道屏障功能,改变菌群组成(如患者体内核心共生菌拟杆菌属的显著减少),引发肠道低度炎症;异常菌群产生的代谢产物通过迷走神经传入通路影响杏仁核、海马体等情绪中枢,形成“脑-肠-脑”的恶性循环[4]。案例中媛媛在心理压力事件后表现出的急性躯体化症状(如突发性颤抖、呼吸急促,蹲下倒地持续30min以上)与慢性功能紊乱(睡眠障碍、学习能力下降),本质上反映了大脑边缘系统与自主神经系统的功能失调。
益生菌的摄入有助于改善肠道屏障、调节免疫反应、降低皮质醇活性,从而缓解HPA轴过度亢进,辅助打破焦虑、抑郁与慢性压力间的恶性循环[5-6]。11 种菌株制剂中的核心菌株脆弱拟杆菌BF839可以改善学习记忆能力和不同环境下的焦虑[7]。朱红硫磺菌作为药食同源真菌,其有效成分三萜类化合物可促进神经营养因子表达与神经突生长,多糖成分则能抑制神经炎症反应[8-9]。鼠李糖乳杆菌可以改善焦虑和抑郁症状[10]。
营养状态的评估为治疗提供了关键靶点。大剂量补充维生素D3-K2与复合镁剂,旨在纠正关键的神经营养缺乏,为神经系统的稳定与修复提供“原料”;复合B族维生素则为线粒体能量代谢和神经递质合成提供全面支持[11]。这种从肠道环境到细胞营养层面的综合调理,旨在打破上述恶性循环,为更高层级的心理治疗和功能恢复奠定了不可或缺的生理基础。
参考文献
[1]Lee E H, Im Kim Y, Geun H G, et al. Effects of academic stress, somatization symptoms, and social support on coping responses in high school students[J]. Journal of the Korean Society of School Health, 2015, 28(2): 56-66.
[2]Uzzan S, Azab A N. Anti-TNF-α Compounds as a Treatment for Depression[J]. Molecules, 2021, 26(8): 2368.
[3]Leite J A, Vieira R S, da Silva J V H, et al. Metabolic Modulation of the Immune-Neuro Axis: Insights into Psychoneuroimmunology[M]//PsychoNeuroImmunology: Volume 1: Integration of Psychology, Neurology, and Immunology. Cham: Springer Nature Switzerland, 2025: 151-186.
[4]Kurhaluk N, Kołodziejska R, Kamiński P, et al. Integrative neuroimmune role of the parasympathetic nervous system, vagus nerve and gut microbiota in stress modulation: a narrative review[J]. International Journal of Molecular Sciences, 2025, 26(23): 11706.
[5]Dziedzic A, et al. The Power of Psychobiotics in Depression: A Modern Approach through the Microbiota-Gut-Brain Axis: A Literature Review. Nutrients. 2024 Apr 4;16(7):1054.
[6]赵宁.补充益生菌改善睡眠剥夺引起的肠道应激损伤的机制研究【D】.华中科技大学,2022(10).
[7]林楚慧,等. 脆弱拟杆菌BF839可改善 Fmr1 KO小鼠的学习记忆能力及社交新奇偏好能力 [J]. 中华神经医学杂志,2022,21(4):341-347.
[8]Hassan K, etl.Neurotrophic and Immunomodulatory Lanostane Triterpenoids from Wood-Inhabiting Basidiomycota. Int J Mol Sci. 2022 Nov 6;23(21):13593.
[9]汪雯翰,刘肖肖,贾 薇,等. 食药用菌抗神经炎症的研究进展[J]. 食用菌学报,2018,25(3):96-102.
[10]Agirman G, Hsiao EY. SnapShot: The microbiota-gut-brain axis. Cell. 2021 Apr 29;184(9):2524-2524.e1.
[11]Maralla S, Bharathi D. Efficiency of Neuro-Nutrient Therapy in the Treatment of Neuropathologies[C]//International Conference On Computational And Bio Engineering. Cham: Springer International Publishing, 2019: 243-253.